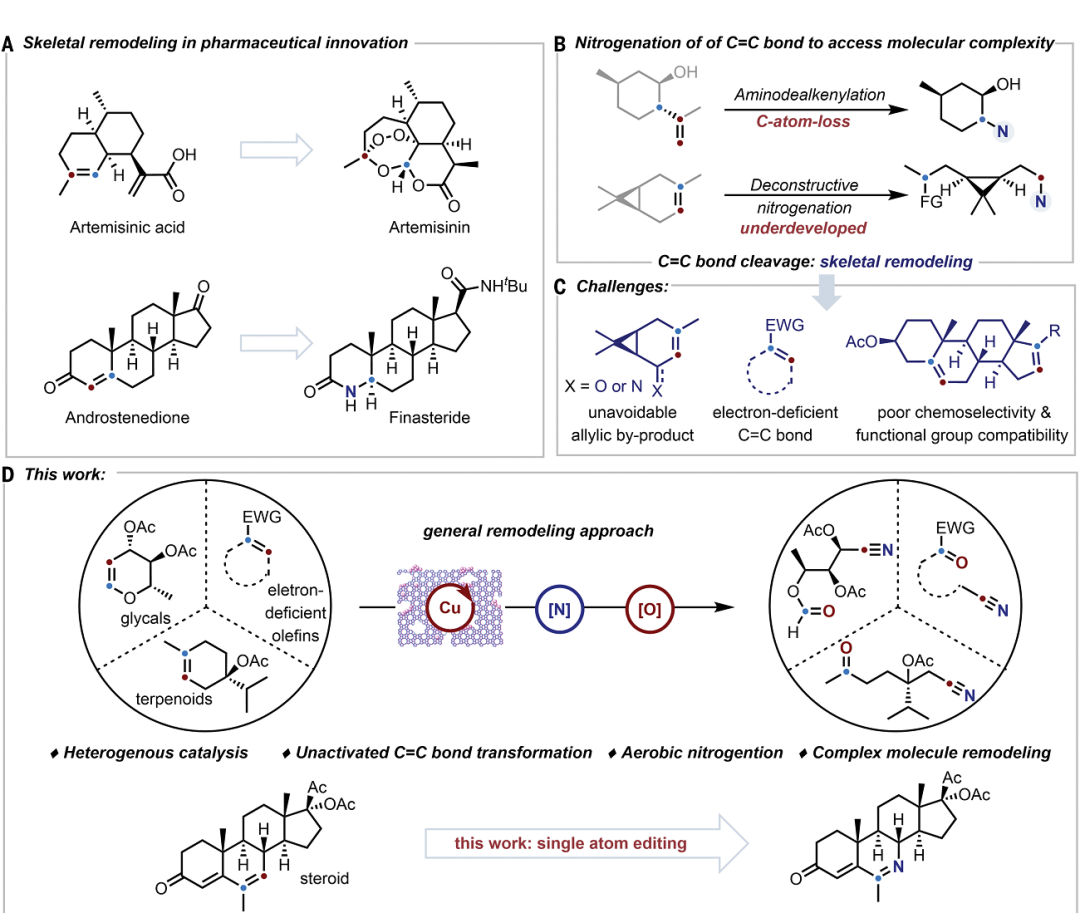
C=C雙鍵的打破和轉化是合成化學和藥物化學領域的重要策略,雖然通過烯烴復分解和臭氧化反應切斷C=C雙鍵在合成天然產物中得到顯著進展,但是仍然缺乏合適的方法切斷C=C雙鍵對分子進行結構重構。
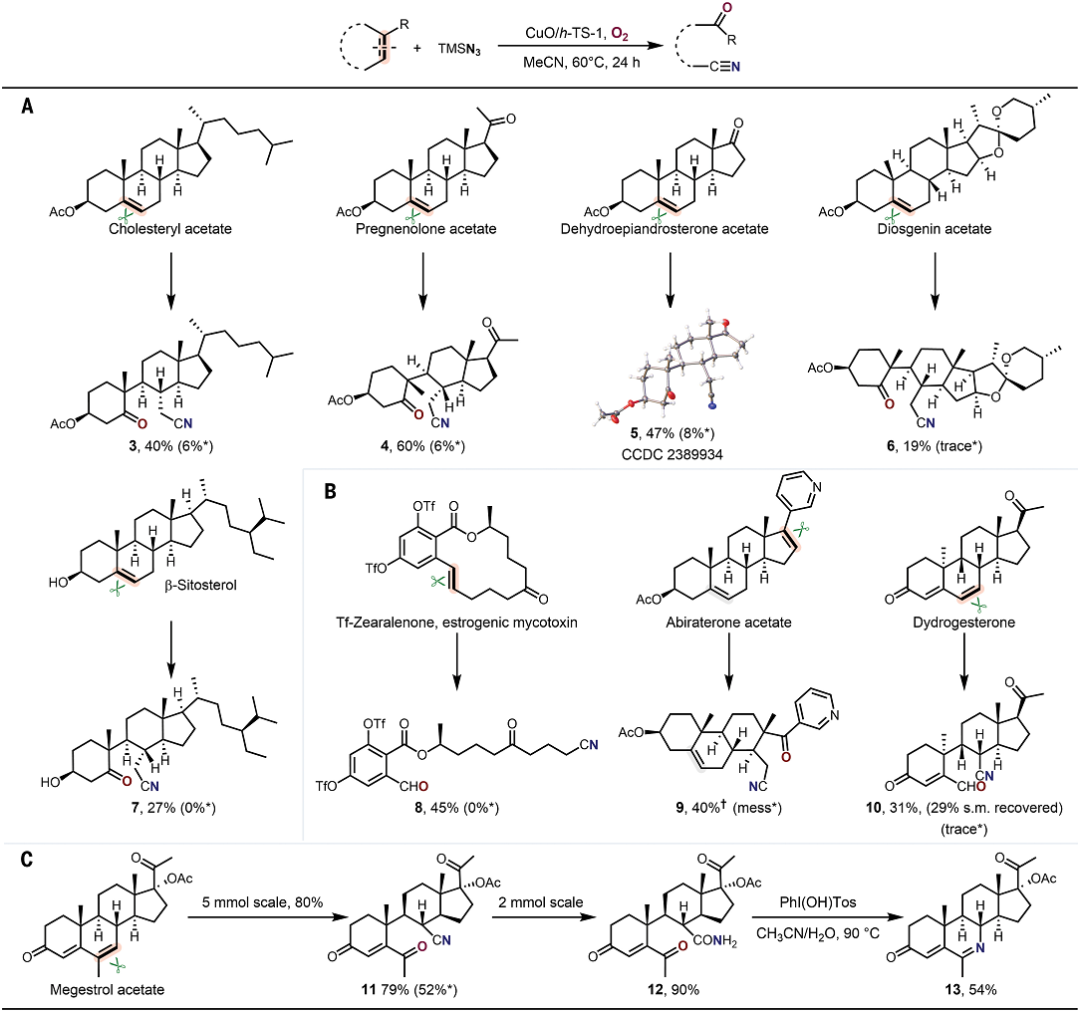
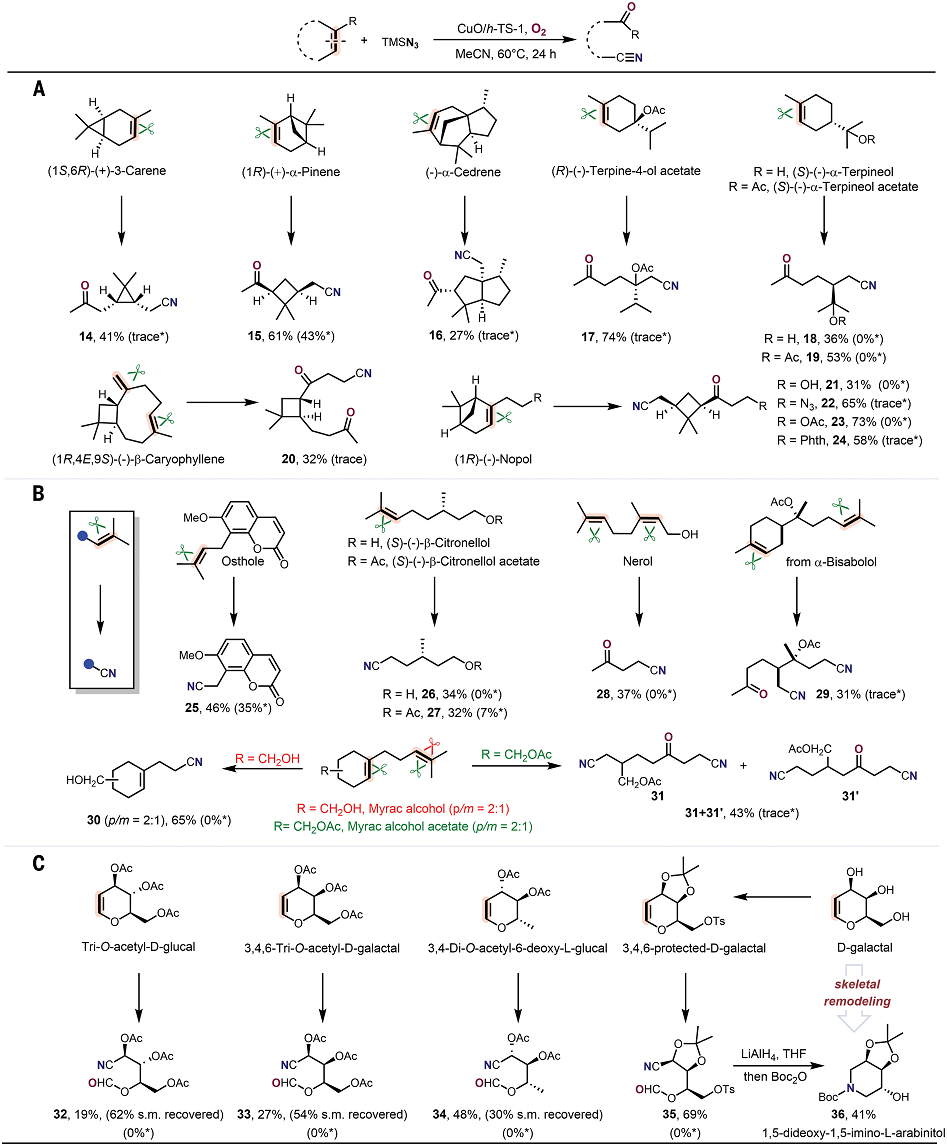
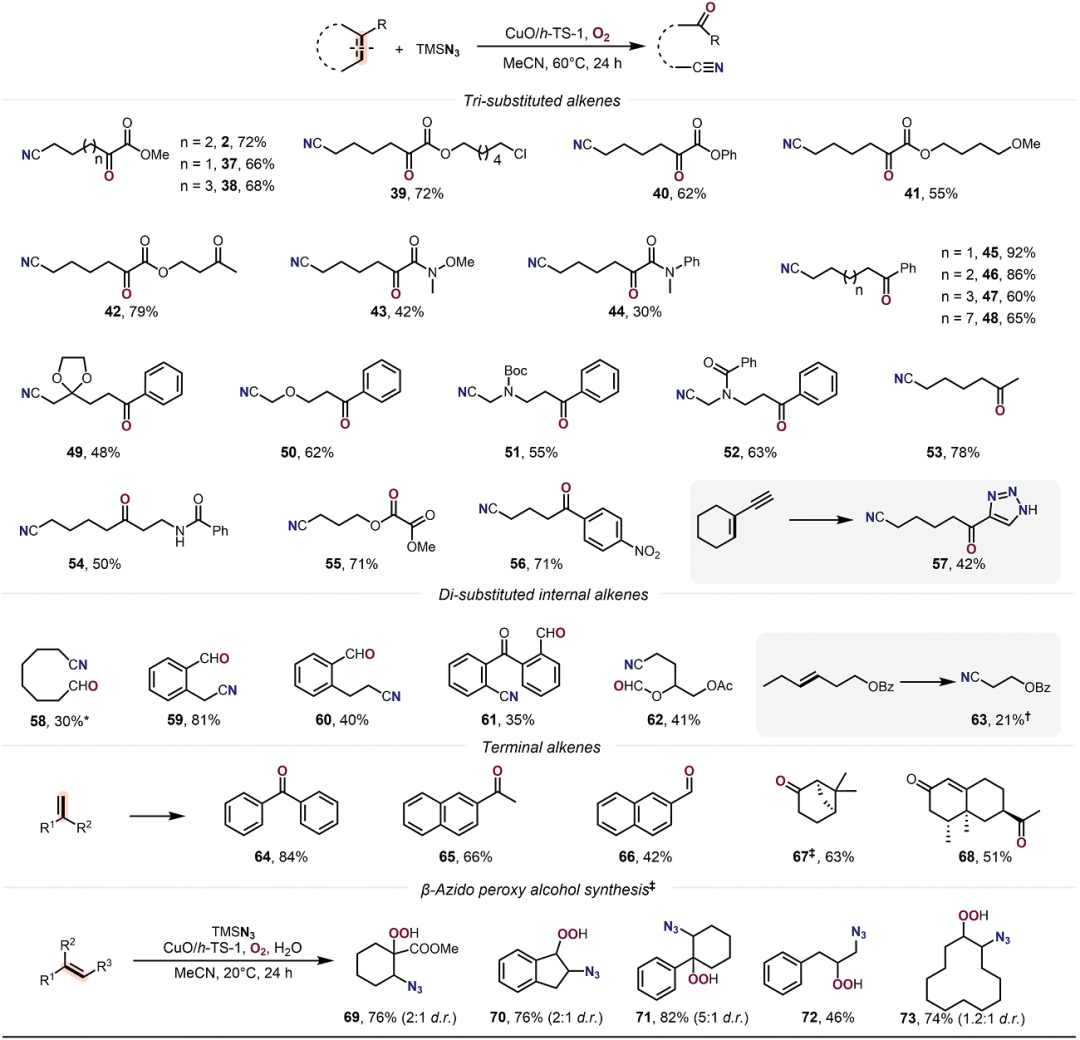
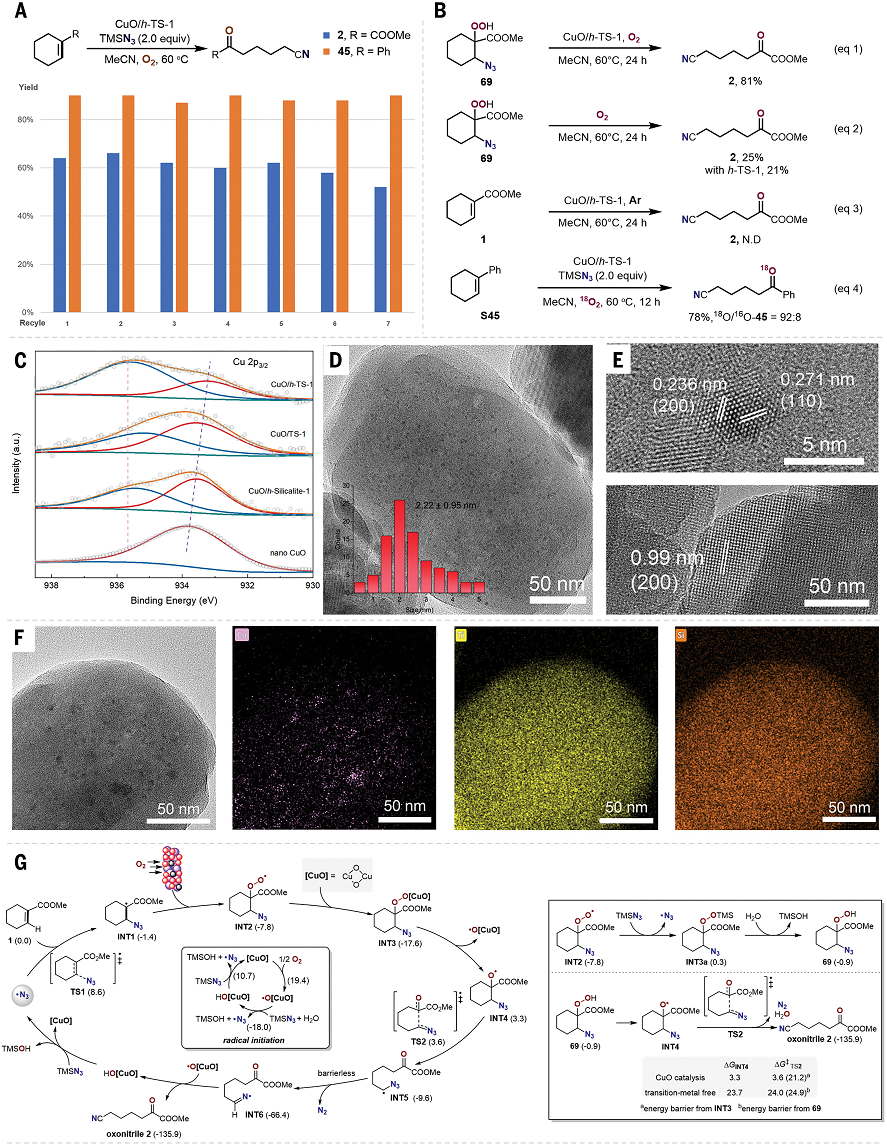
有鑒于此,北京大學焦寧教授、中石化石油化工科學研究院夏長久等報道異相Cu催化切斷C=C雙鍵的策略,能夠將復雜結構分子之中C=C雙鍵任意一側的碳原子轉化為羰基和氰基,因此對復雜分子實現結構重構。 這個方法能夠非常有效的將萜類化合物、糖基、類固醇和生物活性化合物轉化為結構未深入研究的分子結構。這項工作設計了一種可重復使用的異相Cu催化劑(CuO/h-TS-1),在有氧條件下對C=C雙鍵進行氮化,實現了合成高附加值的含氮/含氧化合物(圖1D)。作者能夠轉化多種多樣的C=C雙鍵,包括缺電子烯烴、結構復雜有機分子中的C=C雙鍵。這種方法能夠將以往無法通過TEMPO催化反應轉化,將C=C雙鍵轉化為C=O雙鍵和C≡N三鍵。此外,開發了一種對天然產物和復雜結構化合物的創新切斷C=C雙鍵進行結構重構的策略。目前人們對于切斷C-C化學鍵進行氧化(oxygenation)和氮化(nitrogenation)策略的關注,因此希望開發切斷C=C雙鍵對復雜結構分子進行結構重構,合成氧腈化合物(oxonitriles)。 但是,之前報道的TEMPO催化反應策略存在三個明顯缺點:(i)難以對缺電子烯烴進行親電疊氮自由基加成、(ii)反應的兼容性非常差,無法對結構復雜烯烴(類固醇和萜類化合物)的結構修飾、(iii)催化劑無法回收。為了解決這個缺點,作者提出高效催化劑需要能夠活化疊氮自由基,并且避免自由基犧牲劑。因此,基于這個想法,篩選過渡金屬催化劑。反應條件。對缺電子烯烴1分子測試有氧氮化反應。首先,TEMPO和NHPI作為自由基引發劑和自由基終止劑無法在TMSN3和O2存在下,催化1轉化為氧氮化合物(Table S1,entry 1和2)。使用CoCl2、MgBr2、CuCl2、FeCl2、CuO作為催化劑,只能以較低的產率得到2(Table S1,entry 3-7)。納米粒徑CuO(<50 nm)比塊體CuO表現更好的催化活性(Table S1,entry 7 vs. entry 8)。以上結果表明活性中心的分散性有助于改善催化劑的性能。因此,設計合成一系列過渡金屬催化劑修飾在分子篩載體之中的催化劑(Table S1)。其中,CuO/TS-1催化劑生成2的產率達到64%(Table S1,entry 9)。Fe-氧化物、Co-氧化物、Mn-氧化物修飾的TS-1分子篩無法催化反應(Table S1,entry 10-12)。將CuO擔載到多級結構TS-1(CuO/h-TS-1)之中,得到最好的催化活性,以76%的收率生成2(Table S1,entry 17)。天然產物的優勢結構(privileged scaffolds)具有獨特的化學多樣性和生物相關性,因此是藥物發現領域處于基礎性地位。但是,這些天然產物化合物通常含有豐富的sp3碳和氧原子,以及豐富的氫鍵供體受體,較少的氮原子。因此,氮原子在藥物化學領域非常重要,但是將含氮官能團引入天然分子骨架的方法學非常缺乏。 含氮原子官能團的類固醇分子相比于不含氮原子的結構相比,能夠表現許多功能增強,包括抗菌、抗病毒、抗炎和抗癌活性。在最優的反應條件下,對含有C=C雙鍵的類固醇化合物進行有氧氮化反應(圖2A)。發現這個方法能夠阻礙C-7位點的不利性的烯丙基氧化,選擇性合成一系列其他方法無法得到的高附加值B環修飾5,6-立體結構類固醇化合物(3-7)。 通過X射線晶體表征驗證5的結構。在合適的反應條件下,能夠切斷生成其衍生化的結構(圖2B,8-10)。這種方法能夠對含有C=C雙鍵的萜類化合物進行結構重構(圖3)。對(1S, 6R)-(+)-3-蒈烯(carene)氧化切斷C=C雙鍵生成順式-環丙烷14,產率為41%。類似的,含有環丁烷結構的(1R)-(+)-α-蒎烯(pinene)、(1R)-(–)-諾卜醇(nopol)能夠轉化為手性環丁烷結構,并且含有羥基、疊氮、酯、酰胺官能團(15,21-24)。(–)-α-雪松烯(cedrene)能夠方便的合成結構復雜雙環[3.3.0]辛烷骨架(16),這個結果表明這項方法構筑手性環丙烷、環丁烷、環戊烷和各種官能團的復雜分子。(R)-(–)-4-萜品醇乙酸酯以及衍生物能夠以適中的產率得到含有手性季碳的氧腈化合物(17-19)。(1R, 4E, 9S)-(–)-β-石竹烯(caryophyllene)能夠轉化為反式取代環丁烷衍生物20。這些反應通過TEMPO催化反應方法難以進行。 由于氰基在設計藥物化合物中的重要作用,因此研究萜類化合物的末端異丁烯結構氮化(圖3C)。對蛇床子素、(S)-(–)-β-香茅醇(citronellol)、橙花醇(nerol)、α-紅沒藥醇(bisabolol)等化合物切斷一個或兩個C=C雙鍵能夠合成非環狀烷基腈化合物(25-29)。Myrac alcohol醇以及酯切斷一個或兩個C=C雙鍵能夠生成30,31,31′。糖烯(glycals)能夠轉化為修飾氰基的甲酸酯(32-34)。并且通過TEMPO催化反應過程完全無法進行該反應。該反應能夠通過切斷C=C化學鍵高效率將D-半乳糖烯轉化為1,5-二脫氧-1,5-亞氨基-L-阿拉伯糖醇(圖3C)。這項方法除了能夠轉化結構復雜分子,也能夠用于結構簡單分子的重構(圖4)。對于修飾三個取代基的環狀烯烴,環的尺寸和官能團(苯、鹵、醚、羰基)對反應效率并沒有明顯影響,并且許多缺電子烯烴能夠很好的轉化為氧腈化物(2,37-44)。切斷苯基環己烯或者更大的環狀烯烴能夠以較高的收率生成長鏈氧腈化合物(45-48)。此外,環己烯骨架修飾酸敏感縮酮官能團的反應物能夠以合適的產率生成49。此外,二氫呋喃、N保護的1,2,3,6-四氫吡啶、修飾烷基的環己烯(50-55)能夠方便的轉化。缺電子芳基取代修飾環戊烯以71 %的產率生成56。CuO/h-TS-1通過打破C=C雙鍵和隨后的C≡C點擊反應,能夠以42 %收率生成四唑化合物57。 隨后,對修飾雙取代基的烯烴(環辛烯、茚、二氫萘、5-二苯并辛烯酮)在標準反應條件生成氧腈化合物(58-61)。3,4-二氫-2H-吡喃生成修飾氰基取代基的甲酸酯(62),惰性的線性脂肪烯烴轉化為相應的產物(63)。此外,除了這種環狀烯烴,該反應能夠將端烯烴轉化為酮或者醛(64-68)。此外,在20 ℃和水存在的情況下進行反應,烯烴1的C=C雙鍵不會被切斷,但是能夠生成β-疊氮基過氧醇(69)。此外,該催化反應的優點是CuO/h-TS-1能夠回收,并且不會產生明顯損失。比如,在重復7次催化反應之后,CuO/h-TS-1催化劑的催化活性未見明顯衰減(圖5A)。控制實驗研究反應機理。如圖5B,69反應使用CuO/h-TS-1和h-TS-1轉化反應的產率達到81%和21%。此外,當沒有加入催化劑,在O2氣氛中,69部分轉化為2產物(圖5B,eq 1-2)。這說明CuO/h-TS-1起到主要的作用(圖5B,eq 3)。此外,反應在Ar氣氛中無法發生。以18O2標記,18O-45同位素標記實驗得到78%產率(圖5B,eq 4)。 為了深入理解CuO/h-TS-1的催化反應性能,進行多種表征實驗。通過XPS表征Cu的氧化態(圖5C),發現CuO/h-S-1、CuO/TS-1、CuO/h-TS-1的氧化態都是+2價態。此外,通過TEM表征CuO顆粒在h-TS-1內的分布均勻性,結果表明樣品沒有塊體CuO或者較大CuO納米粒子(圖5C-F)。h-TS-1的豐富多孔結構有助于分子篩內的擴散傳質。通過DFT理論計算研究反應機理,發現反應的關鍵是Cu促進切斷O-O化學鍵的步驟(圖5G)。這項研究為構筑更加豐富化學空間用于拓展合成化學和藥物發現領域提供強有力的策略。Zengrui Cheng et al. , Catalytic remodeling of complex alkenes to oxonitriles through C=C double bond deconstruction.Science387,1083-1090(2025).DOI: 10.1126/science.adq8918https://www.science.org/doi/10.1126/science.adq8918